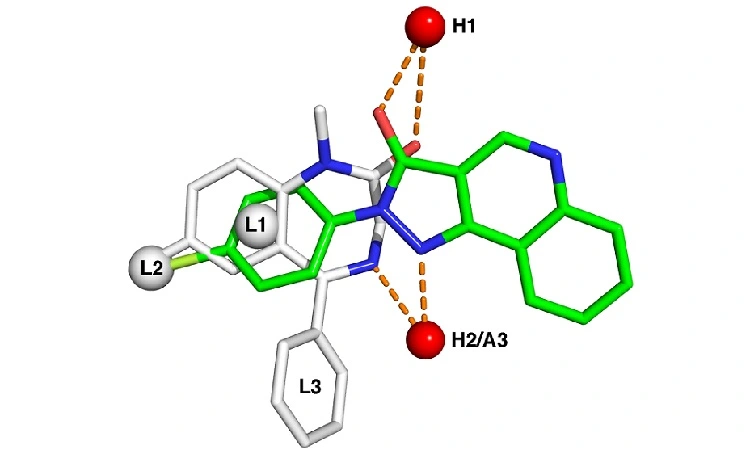
Что такое Фармакофор?
Фармакофор — это центральное понятие в молекулярной фармакологии и лекарственной химии, которое используется для понимания и прогнозирования взаимодействий между молекулой (например, лекарственным веществом) и её биологической мишенью.
Основные характеристики фармакофора
- Химические свойства:
- Гидрофобные области: Части молекулы, которые притягиваются к липофильным участкам биологической мишени.
- Полярные группы: Доноры и акцепторы водородных связей.
- Электростатические взаимодействия: Заряженные участки молекулы могут взаимодействовать с противоположно заряженными частями биологической мишени.
- Ароматические взаимодействия: π-π-стэкинг, взаимодействие между плоскими ароматическими кольцами молекулы и мишени.
- Пространственное расположение:
- Для успешного связывания молекула должна иметь определённое пространственное распределение своих химических свойств. Например, гидрофобные и полярные группы должны быть расположены на правильных расстояниях друг от друга.
Как определяется фармакофор?
- Экспериментальные данные:
- Используются данные о молекулах, которые взаимодействуют с целевой мишенью. Анализируются сходства между активными соединениями для выявления общих структурных элементов.
- Молекулярное моделирование:
- Современные компьютерные методы, такие как докинг, молекулярная динамика и кристаллографический анализ, позволяют исследовать взаимодействие молекулы с мишенью и выделять ключевые элементы.
- Фармакофорные модели:
- Создаются абстрактные 3D-модели, включающие ключевые химические свойства и их пространственное расположение.
Применение фармакофора
- Разработка лекарств:
- На основе фармакофора можно проектировать новые соединения, которые имеют высокую вероятность взаимодействия с целевой молекулой.
- Например, если известен фармакофор ингибитора фермента, можно синтезировать новые аналоги с похожими характеристиками.
- Виртуальный скрининг:
- Используется в базах данных соединений для поиска молекул, которые соответствуют заданному фармакофору.
- Оптимизация соединений:
- После нахождения активных соединений фармакофор помогает оптимизировать их, улучшая связывание и биодоступность.
Рассмотрим пример фармакофора для ингибиторов протеазы вируса иммунодефицита человека (ВИЧ-протеазы). Это фермент, который разрезает белковые прекурсоры вируса на функциональные белки, необходимые для его размножения. Блокировка ВИЧ-протеазы предотвращает созревание вируса, что делает её важной мишенью для антиретровирусной терапии.
Шаг 1: Анализ мишени
- Мишень: ВИЧ-протеаза — димерный фермент, активный центр которого содержит аспартатные остатки, участвующие в каталитическом процессе.
- Задача: Создать молекулу, которая эффективно блокирует активный центр фермента.
Шаг 2: Определение фармакофора
- Ключевые элементы взаимодействия:
- Гидрофобные карманы: В активном центре фермента есть участки, которые связываются с гидрофобными частями молекулы.
- Полярные группы: Водородные связи с аспартатами активного центра.
- Электростатические взаимодействия: Некоторые ингибиторы содержат заряженные группы, которые взаимодействуют с ферментом.
- Пространственная структура:
- Полярные и гидрофобные элементы должны быть расположены так, чтобы идеально вписаться в активный центр.
Шаг 3: Создание фармакофорной модели
На основе известных ингибиторов ВИЧ-протеазы (например, ритонавира или лопинавира) выявляются ключевые элементы:
- Гидрофобные группы:
- Эти группы взаимодействуют с гидрофобными областями активного центра (например, бензольные кольца или алифатические цепи).
- Водородные связи:
- Полярные группы (например, гидроксильные) образуют водородные связи с каталитическими остатками аспартата.
- Гибкие связи:
- Некоторые молекулы имеют гибкие соединения, которые позволяют им адаптироваться к форме активного центра.
Шаг 4: Пример фармакофора
Фармакофорная модель ингибитора ВИЧ-протеазы может выглядеть так:
- Гидрофобные области: Две области, соответствующие карманам активного центра.
- Полярные точки взаимодействия: Две донорские группы для водородных связей с остатками аспартата.
- Гибкость: Связи, позволяющие молекуле адаптироваться к форме мишени.
Эта модель используется для поиска новых соединений, которые соответствуют описанным свойствам.
Шаг 5: Применение модели
- Виртуальный скрининг:
- Используя фармакофор, тысячи молекул из базы данных проверяются на соответствие модели.
- Те соединения, которые соответствуют фармакофору, считаются перспективными и тестируются дальше.
- Оптимизация:
- После получения первых активных соединений их структура модифицируется, чтобы повысить активность и специфичность.
Пример реализации
- Ритонавир: У него есть гидрофобные группы (ароматическое кольцо), взаимодействующие с гидрофобными карманами, и гидроксильная группа, образующая водородные связи с аспартатами.
- Модификация фармакофора ритонавира помогла разработать другие препараты, такие как лопинавир, с улучшенной активностью.
Пример фармакофора
Рассмотрим ингибитор ацетилхолинэстеразы (АХЭ), фермента, разрушающего ацетилхолин:
- Катионная группа (например, четвертичный аммоний) взаимодействует с анионным участком в активном центре фермента.
- Гидрофобная цепь, связывающаяся с гидрофобным карманом фермента.
- Электронодонорная группа, способная образовывать водородную связь с остатками фермента.
Преимущества использования фармакофоров
- Экономия времени: Позволяет избежать дорогостоящих и длительных лабораторных экспериментов.
- Универсальность: Может применяться к различным классам мишеней.
- Прогнозирование активности: На основе фармакофора можно оценивать биологическую активность новых соединений.